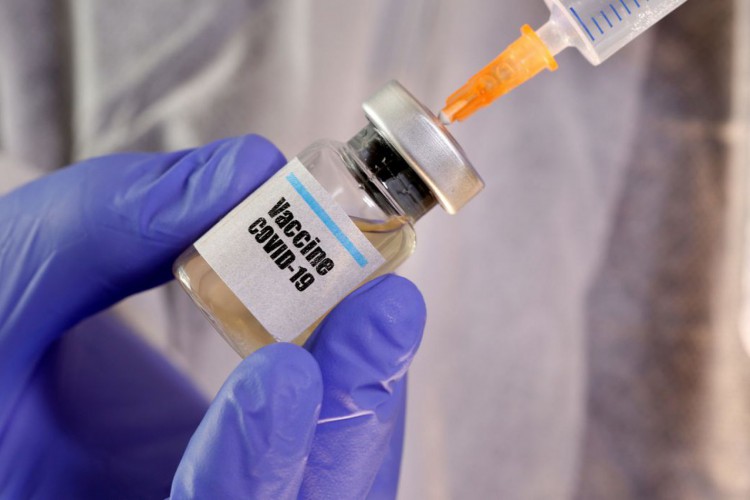
O teste da vacina Oxford é suspenso depois que um voluntário apresenta um “efeito adverso sério”. A paralisia é um “procedimento padrão” e visa garantir a eficácia e total segurança da vacina para humanos (Foto: Arquivo)
Estudos Universidade de Oxford para o desenvolvimento de um vacina para o novo coronavírus, que causa COVID-19, foram temporariamente suspensos no Reino Unido nesta terça-feira 8. O pedido de suspensão feito pela empresa responsável pela produção da vacina foi estendido a todos os países que testaram a população, inclusive o Brasil. A medida ocorreu depois que um dos voluntários na fase de teste teve um “efeito adverso sério”.
A ação para interromper a investigação e a última fase de testes do produto que visa garantir a imunização contra a Covid-19 é um “procedimento padrão”, segundo a multinacional biofarmacêutica AstraZeneca, coordenadora dos testes, em aliança com a Oxford. A suspensão de testes e estudos clínicos visa garantir que equipes de pesquisadores possam investigar a fundo a ocorrência de uma reação à vacina. A medida visa garantir a máxima eficácia da vacina, bem como sua segurança para o ser humano.
A Agência Nacional de Vigilância Sanitária (Anvisa), responsável por autorizar os testes de vacinas no Brasil, confirmou por meio de nota oficial enviada ao G1 que foi notificada pela AstraZeneca com pedido de suspensão dos testes. A vacina Oxford, como ficou conhecida, é a principal aposta do governo brasileiro diante da pandemia do coronavírus.
A entidade indicou que estava aguardando informações mais detalhadas sobre o caso da reação adversa, para poder se posicionar antes da suspensão dos testes no Brasil, a pedido dos órgãos responsáveis pela vacina, ou não. “A decisão de descontinuar os estudos foi tomada pelo laboratório, que a comunicou aos países participantes. A Anvisa já recebeu a mensagem e vai aguardar o envio de mais informações para se pronunciar oficialmente ”, refletiu a agência em nota oficial.
Ocorreu o anúncio de suspensão da prova horas depois o ministro interino da Saúde, Eduardo Pazuello, afirmou que até janeiro de 2021 a campanha de vacinação contra a Covid-19 seria implementada no Brasil. O país planeja investir cerca de R $ 1,9 bilhão para participar do desenvolvimento e obter os direitos de fabricação da vacina.
Em comunicado divulgado à imprensa inglesa e à CNN, a sede da AstraZeneca no Reino Unido anunciou que: “Esta é uma ação de rotina que deve ocorrer sempre que houver uma doença potencialmente inexplicada em um dos julgamentos, durante a investigação, garantindo a manutenção a integridade das evidências ”.
A empresa garantiu que a suspensão é temporária e não indica falha no desenvolvimento da vacina, já que este é o primeiro caso relatado de reações adversas ao imunizante que está sendo produzido contra o vírus causador do Covid-19, SARS -COV- 2. “Nosso processo de revisão padrão causou uma pausa na vacinação para permitir a revisão dos dados de segurança”, acrescentou ele em um comunicado.
A empresa ressaltou ainda que está transferindo todos os profissionais de suas unidades para analisar o caso, a fim de minimizar os efeitos negativos no cronograma de lançamento das vacinas. “Estamos comprometidos com a segurança de nossos participantes e com os mais altos padrões de conduta em nossos testes”, concluiu o comunicado da empresa.
Se a fase atual de testes da vacina Oxford for concluída com sucesso e os resultados forem satisfatórios, a vacina desenvolvida pode ser disponibilizada às agências reguladoras, para que possam revisar todos os estudos, testes e procedimentos para o desenho da vacina. a fim de atestar seu funcionamento e segurança e, posteriormente, autorizar a produção em larga escala e imunização da população.


:quality(70):focal(836x315:846x325)/cloudfront-ap-southeast-2.images.arcpublishing.com/tvnz/3CABZGH6INEJFGNLZHFE73X45Y.jpg)
